Dario Sannino commenta lo straordinario studio dell’università di Basilea.
La metastasi è la diffusione delle cellule tumorali dalla zona corporea in cui si sono formate per la prima volta (massa primaria) ad un’altra parte del corpo. Nelle metastasi, le cellule tumorali si staccano dalla massa primaria, viaggiano attraverso il sistema sanguigno o linfatico e formano una nuova massa tumorale in altri organi o tessuti del corpo.
Ricerche precedenti hanno dimostrato che le cellule tumorali circolanti (CTC) sono la fonte delle metastasi. Le CTC vengono eliminate dai tumori e circolano nel flusso sanguigno. Questo processo può verificarsi anche in una fase iniziale del cancro. Tuttavia, i fenomeni biologici che innescano lo spargimento dei cluster CTC da una lesione cancerosa primaria non sono completamente compresi. Ora i ricercatori dell’Università di Basilea riferiscono che la mancanza di ossigeno è responsabile della separazione dei cluster CTC dalla massa tumorale primaria.
I loro risultati, “Hypoxia Triggers the Intravasation of Clustered Circulating Tumor Cells“, sono stati pubblicati sulla rivista Cell Reports e sono stati guidati da Nicola Aceto, PhD, assistente professore della Swiss National Science Foundation e capogruppo del Cancer Metastasis Lab presso l’Università di Basilea.
“Quando si marcano dinamicamente le cellule di cancro al seno lungo la progressione del cancro, si osserva che la maggior parte dei cluster CTC è in fase di ipossia, mentre le singole Cellule Tumorali Circolanti sono in gran parte normossiche”, hanno osservato i ricercatori.
Lo studio condotto su ratti, ha analizzato l’apporto di ossigeno all’interno dei tumori, il distacco delle CTC e le loro proprietà biologiche molecolari e cellulari. I ricercatori hanno osservato che le diverse aree del tumore ricevono livelli differenti di ossigeno.
Cellule cancerose con mancanza di ossigeno sono state trovate ovunque il tumore avesse un numero relativamente inferiore di vasi sanguigni. I ricercatori hanno quindi studiato i cluster CTC che si erano separati dalle masse tumorali primarie e hanno scoperto che soffrivano anch’esse di mancanza di ossigeno.
I ricercatori hanno concluso che le cellule lasciano il tumore primario se non ricevono abbastanza ossigeno. “È come se troppe persone fossero ammassate insieme in un piccolo spazio. Alcuni usciranno per prendere un po’d’aria fresca”, ha spiegato Dario Sannino.
Ulteriori osservazioni hanno rivelato che i cluster CTC con una mancanza di ossigeno hanno formato metastasi più velocemente e hanno ridotto il tempo di sopravvivenza dei ratti rispetto ai cluster con un contenuto di ossigeno normale. E’ quindi altamente probabile che se un tumore non ha abbastanza ossigeno, i cluster CTC si separeranno dalla massa tumorale primaria.
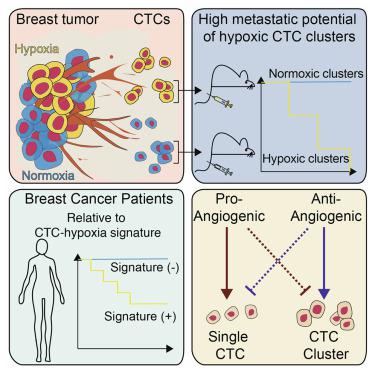
“In un tumore, ci si aspetta generalmente che l’ipossia sia limitata al nucleo e all’interno di regioni scarsamente vascolarizzate. Tuttavia, questo è un apparente paradosso nel contesto della biologia delle metastasi perché le cellule tumorali metastatiche devono avere accesso a vasi sanguigni funzionali per ottenere la diffusione. Abbiamo pensato di affrontare questa controversia affrontando direttamente il ruolo dell’ipossia nei modelli di metastasi spontanee in vivo e in relazione alla generazione e metastasi di CTC”, hanno spiegato i ricercatori.
I ricercatori hanno stimolato la formazione di vasi sanguigni, per aumentare l’apporto di ossigeno alle cellule tumorali. Come previsto, il numero di cluster CTC di separazione è diminuito, i ratti hanno formato meno metastasi e hanno vissuto più a lungo, tuttavia, le dimensioni del tumore primitivo sono aumentate in modo significativo.
“Questo è un risultato provocatorio”, ha aggiunto Dario Sannino. “Se diamo abbastanza ossigeno al tumore, le cellule cancerose non hanno motivo di lasciare il tumore e metastatizzare. D’altra parte, questo accelera la crescita del tumore primario”. Andando avanti, i ricercatori non vedono l’ora di applicare i loro risultati in un contesto clinico in cui le caratteristiche del cancro variano da paziente a paziente. Le loro scoperte potrebbero portare a nuove strategie di trattamento per il cancro. “Noi ipotizziamo che le terapie volte a ridurre l’ipossia intra-tumorale, da sole o in combinazione con agenti antitumorali, possano fornire una nuova opportunità per smorzare la diffusione metastatica del cancro nei pazienti con cancro al seno”, hanno concluso i ricercatori.
Dott. Dario Sannino
Corporate Quality Sr. Manager at Bracco Imaging S.p.A.